Die Anforderungen ISO 13485 dienen dazu, gesetzliche Forderungen im Bereich der Medizinprodukte – beispielsweise aus dem Medizinproduktegesetzt MPG – zu erfüllen und knüpft an die Struktur der ISO 9001 an. Damit Medizinproduktehersteller ein neues Qualitätsmanagementsystem gemäß ISO 13485 erfolgreich implementieren oder ein bereits bestehenden QM-System sicher aufrechterhalten können, müssen sie über ein fundiertes Basiswissen hinsichtlich der Anforderungen der ISO 13485 sowie des Medizinproduktegesetztes verfügen.
In diesem ISO 13485 Seminar erfahren Sie, welche Qualitätsmaßnahmen für ein Qualitätsmanagementsystem nach ISO 13485 aufbauend auf die ISO 9001 notwendig sind und welche Anforderungen sich aus der Norm ISO 13485 ergeben sowie welche Dokumentationspflichten hierfür erforderlich sind.
Sie lernen in dieser Basiswissen Ausbildung ISO 13485 alle Aspekte der Qualitätsmanagementnorm für Medizinproduktehersteller im Detail kennen und lernen die Forderungen, die diese mit sich bringt kennen. Außerdem wird Ihnen in dieser Ausbildung ISO 13485 Basiswissen – MPG Weiterbildung das nötige Wissen ermittelt, um eine technische Dokumentation, welche Bezug auf die Richtlinien des Medizinproduktgesetzes nimmt, zu erarbeiten.

Welche Inhalte vermitteln wir Ihnen in diesem Basiswissen ISO 13485 Seminar?
Nachfolgend erhalten Sie eine detaillierte Übersicht der Inhalte dieser Basiswissen Schulung zu den ISO 13485 Anforderungen. Dabei profitieren Sie, durch einen ausgewogenen Mix aus Theorie- und Übungseinheiten, vom maximalen Praxistransfer.
Was bedeutet Qualitätsmanagement für Medizinproduktehersteller?
Zuerst beschäftigen wir uns mit den Grundlagen und Hintergründen des Qualitätsmanagements für Medizinproduktehersteller.
- Einführung und geschichtliche Entwicklung
- QM Normen anwenden um gesetzliche Forderungen zu erfüllen
- Prozessorientierter Ansatz der neuen Normen ISO 9001 und ISO 13485
Welche Norm Anforderungen stellt die ISO 13485?
In dieser Einheit lernen Sie die ISO 13485 im Detail kennen. Dabei werden neben dem Inhalt ebenfalls Anwendungsbereiche sowie Ausschlussmöglichkeiten sowie die erweitere Dokumentation im Bereich Qualitätsmanagement Medizinprodukte gelernt.
- Inhalt und Struktur
- Bereiche der Anwendung und Ausschlüsse
- Erweiterte Forderungen der Norm an Aufzeichnungen und Dokumentation
- Die Qualitätsmanagement Norm ISO 13485 im Unternehmen konsequent umsetzen
Qualitätsmanagement Medizinprodukte – wie verläuft die technische Dokumentation?
Für Medizinproduktehersteller ist die technische Dokumentation von besonderer Bedeutung – alles was Sie hierfür wissen müssen, erfahren Sie hier.
- Technische Dokumentation im EG-Recht und in anderen Gebieten
- Bedeutung der Technischen Dokumentation im Konformitätsbewertungsverfahren sowie in der Marktüberwachung
- Richtlinie 93/42/EWG – Anforderungen an die Technische Dokumentation
- Inhalte, möglicher Aufbau, verwendete Sprachen, Lenkung und Verfügbarkeit
- Technische Dokumentation bei OEM-Produkten
Das Medizinproduktegesetz MPG im Detail
Nicht nur die Norm ISO 13485 sondern ebenfalls das Medizinproduktegesetz spielen eine immense Bedeutung für Medizinproduktehersteller. Dabei werden auch die speziellen Anforderungen für Händler und Importeure in Augenschein genommen.
- Die europäischen und deutschen Richtlinien des MPG
- Spezielle Anforderungen an Herstellung, Vertrieb sowie Import / Export
- Hersteller, Händler und Importeure – Verantwortlichkeiten und Pflichten
- Schnittstellen zu Betreibern und Konsumenten von Medizinprodukten bestimmen
Welche Voraussetzungen gelten für Ihre Teilnahme an diesem ISO 13485 Seminar zu den Anforderungen ISO 13485?
Es sind dabei keine speziellen Kenntnisse zur Teilnahme an diesem ISO 13485 Seminar erforderlich.
Wer ist die Zielgruppe dieser Ausbildung?
Diese Basiswissen Schulung ISO 13485 richtet sich dabei an Qualitätsmanagementbeauftragte, Unternehmensleitung sowie sonstiges Fachpersonal im QM-Bereich. Aber auch Händler, Hersteller und Importeure von Medizinprodukten aus den Bereichen Zulassung, Regulatory Affairs, Qualitätsmanagement sowie Dienstleister aus der Medizinproduktbranche, die ein QM-System nach ISO 13485 einführen oder dauerhaft betreuen wollen.
Welches Ziel verfolgt dieses ISO 13485 Seminar?
Wir vermitteln Ihnen in dieser Schulung das fundierte Wissen zu den Anforderungen der ISO 13485 – Qualitätsmanagement Medizinprodukte. Sie lernen zudem die gesetzlichen Forderungen des MPG kennen und wissen, wie Sie Rechtssicherheit für das eigene Unternehmen erlangen können.
Was für einen Schulungsnachweis gibt es im Anschluss an Ihre Teilnahme?
Sie erhalten eine Qualifikationsbescheinigung zur Teilnahme an dem Kurs „Basiswissen ISO 13485 Qualitätsmanagement Medizinprodukte“ in deutscher sowie englischer Ausführung.
Alle Informationen zu dieser Ausbildung ISO 13485 Basiswissen
 Weitere Infos, Termine & Anmeldung
Weitere Infos, Termine & Anmeldung
Hier erhalten Sie Infos zu den Preisen, den nächsten Terminen und den Veranstaltungsorten in Ihrer Nähe! Sie möchten diese Schulung besuchen? Dann melden Sie sich gleich zu Ihrem Wunschtermin an!
 Download der Schulungsinhalte
Download der Schulungsinhalte
Laden Sie sich die Inhalte der Ausbildung bequem und kostenfrei als PDF-Datei herunter. Informieren Sie sich über diese und viele weitere Schulungen aus unserem Ausbildungsprogramm!
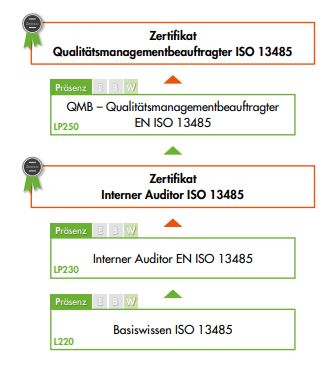
QM Medizinprodukte ISO 13485 Ausbildung – Ihre Übersicht
Unsere Ausbildungsgrafik zeigt Ihnen alle Schulungen unserer QM Ausbildung nach ISO 13485. Welche Seminare für Sie die Richtigen sind, entscheidet sich schließlich anhand Ihrer Vorkenntnisse und Ihrer Ziele. Wir beraten Sie selbstverständlich gerne dabei!
DOWNLOAD Ausbildungsprogramm: Klicken Sie auf den Link, um sich unsere umfangreiche Übersicht als PDF herunterzuladen. Hier finden Sie unser ausführliches Seminarprogramm mit vielen weiteren Ausbildungslinien für Ihr Qualitätsmanagement Medizinprodukte.
Zudem sehen Sie auf einen Blick, welche Möglichkeiten Sie bezüglich der Schulungsform haben. Unsere Fortbildungen können alle als Präsenzschulungen gebucht werden, mitunter aber auch als Blended Learning und E-Learning Kurs.
Klicken Sie auf die Grafik, um diese vergrößert anzuzeigen.